Willkommen im
Psychose & Schizophrenie - Forum
Medizinisch fundierte Informationen zu Orientierung, Medikation und Therapie.
Für Betroffene, Angehörige sowie fachlich Interessierte.
Chat und Komfortfunktionen für angemeldete User.
Stabilisierung mithilfe von Bupropion
Übersicht zu Intervalltherapie, Kombinationsstrategien und Nebenwirkungsprofilen.
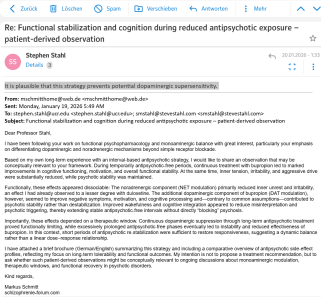
“It is plausible that this strategy prevents potential dopaminergic supersensitivity.”
– Prof. Dr. Stephen M. Stahl
➝ Grafische Übersicht: Schizophrenie‑Netzwerk
➝ Die Dopamin‑Regulationshypothese
➝💙 Schizophrenie für Angehörige – einfach, respektvoll und verständlich erklärt
Registrierung – Kostenfrei und Anonym.
individuelle Tipps – Ratschläge – Unterstützung.
Medikamentöse Orientierung bei Psychose – Schizophrenie (Langfassung)
- Aufrufe Aufrufe: 9.410
- Letzte Aktualisierung Letzte Aktualisierung:
- Umleiten Weitergeleitet von 💊 Medication Recommendation for Psychosis – Schizophrenia – Short Version
-
Inhalt
- Medikamentöse Orientierung bei Psychose und Schizophrenie (Langfassung)
 Intervalltherapie bei Schizophrenie:
Intervalltherapie bei Schizophrenie:- Intervallbasierte Kombination aus antipsychotischer Stabilisierung und kontinuierlicher Modulation
 Broschüre-Kurzfassung-2-seitig
Broschüre-Kurzfassung-2-seitig Broschüre-short-version-2-pages (English)
Broschüre-short-version-2-pages (English) 1. Die Therapieform: Intervalltherapie + Bupropion (praxisnah erklärt)
1. Die Therapieform: Intervalltherapie + Bupropion (praxisnah erklärt)- 1.1 Grundidee
- 1.2 Zeiträume der Intervalltherapie
 ASCII‑Diagramm: Intervallzyklus
ASCII‑Diagramm: Intervallzyklus- 1.3 Warum funktioniert das? (Kurzüberblick)
- 1.4 Was passiert in der Aripiprazol‑Phase?
- 1.5 Was passiert in der Absetzphase?
 2. Die Wirkstoffe im Überblick (praxisnah)
2. Die Wirkstoffe im Überblick (praxisnah)- 2.1 Aripiprazol (kurzzeitig)
- 2.2 Bupropion (kontinuierlich)
- 2.3 SSRI
- 2.4 Trizyklische Tropfen (Trimipramin, Doxepin)
- 2.5 Trazodon
- 2.6 Ergänzungen (kurz)
 3. Mechanismen (einfach, getrennt, dann zusammengeführt)
3. Mechanismen (einfach, getrennt, dann zusammengeführt)- 3.1 NET – Noradrenalin
- 3.2 DAT – Dopamin
- 3.3 Partialagonismus (Aripiprazol)
- 3.4 Zusammenspiel
 4. Intervalllogik – warum dieses Modell funktioniert
4. Intervalllogik – warum dieses Modell funktioniert- 4.1 Warum kurze Aripiprazol‑Phasen ausreichen
- 4.2 Warum lange Absetzphasen möglich sind
- 4.3 Warum sich die Intervalle im Verlauf verkürzen
- 4.4 Warum dies ein therapeutischer Fortschritt ist
- 4.5 Warum Antidepressiva „resetten“
- 4.6 Warum Bupropion irgendwann „zu wenig“ wird
- 4.7 Warum Schlafstörungen ein Frühwarnsignal sind
- 4.8 Warum sich die Symptome nach dem Reset wieder beruhigen
 5. Nahrungsergänzung – funktionell und gezielt eingesetzt
5. Nahrungsergänzung – funktionell und gezielt eingesetzt- 5.1 Vitamin B6
- 5.2 Magnesium
- 5.3 B‑Komplex
- 5.4 Sulforaphan
- 5.5 Lithium‑Orotat
 6. Funktionelle Gesamtordnung – die „große Landkarte“
6. Funktionelle Gesamtordnung – die „große Landkarte“- 6.1 Dopamin – Salienz, Integration und Denktempo
- 6.2 Noradrenalin – Stress, Reizbarkeit und Impulsivität
- 6.3 Glutamat – Präzision und Vorhersagefehler
- 6.4 GABA – Hemmung und Stabilität
- 6.5 Neuroinflammation – ein modulierender Faktor
- 6.6 Rezeptorsensitivität – Anpassung statt Fixierung
 7. Nebenwirkungsprofile atypischer Antipsychotika
7. Nebenwirkungsprofile atypischer Antipsychotika 8. Fazit – ein funktionelles Weiterdenken klassischer Therapie
8. Fazit – ein funktionelles Weiterdenken klassischer Therapie- Kontinuierliche Einnahme von Bupropion (NDRI)
- Wirkung auf Symptome
- Antipsychotische Komponente im therapeutischen Fenster
- NET‑Wirkung und innere Unruhe
- Einnahmestruktur und Dosisentwicklung
- Schlafstörungen und Abgrenzung zu Frühwarnsymptomen
 Medikamentenplan – funktionelle Übersicht
Medikamentenplan – funktionelle Übersicht- 1. Hauptmedikation – tragende Säulen der Intervalltherapie
- 2. Begleitmedikation – symptomorientierte Ergänzung
- 3. Nahrungsergänzung – funktionell priorisiert
 Artikel Druckansicht
Artikel Druckansicht
Diese Langfassung bietet eine sachliche medikamentöse Orientierung bei Psychose und Schizophrenie. Sie beschreibt Wirkprinzipien, Einsatzbereiche und Grenzen verschiedener Behandlungsansätze und dient der Einordnung therapeutischer Konzepte – ohne individuelle Therapieempfehlung.
Die dargestellte Orientierung richtet sich an Menschen mit Psychose oder Schizophrenie, die unter klassischen Dauermedikations‑Strategien zwar symptomatisch stabil sind, jedoch funktionell eingeschränkt bleiben oder eine dauerhafte antipsychotische Behandlung nicht tolerieren.
Autor: Markus („Maggi“)
Letzte Aktualisierung: Februar 2026
Medikamentöse Orientierung bei Psychose und Schizophrenie (Langfassung)
 Intervalltherapie bei Schizophrenie:
Intervalltherapie bei Schizophrenie:Intervallbasierte Kombination aus antipsychotischer Stabilisierung und kontinuierlicher Modulation
Das hier beschriebene Intervallmodell verfolgt einen funktionellen Ansatz, der Stabilisierung und langfristige Belastbarkeit miteinander verbindet. Es kombiniert eine kurzzeitige antipsychotische Stabilisierung mit einer kontinuierlichen funktionellen Modulation.
Ziel ist eine stabile Symptomkontrolle ohne dauerhafte Antipsychotika‑Belastung, mit dem Potenzial für bessere Langzeitverläufe, höhere Lebensqualität und eine geringere Nebenwirkungsbelastung als unter klassischen Dauermedikations‑Regimen.
Dieses Modell versteht sich nicht als Ersatz etablierter Therapien, sondern als deren funktionelle Weiterentwicklung, insbesondere für Patientinnen und Patienten, bei denen herkömmliche Behandlungsansätze an ihre Grenzen stoßen.
 Broschüre-Kurzfassung-2-seitig
Broschüre-Kurzfassung-2-seitig Broschüre-short-version-2-pages (English)
Broschüre-short-version-2-pages (English)
Dieses Kapitel ist bewusst einstiegsfreundlich formuliert. Es soll Ärzt*innen wie Betroffenen ermöglichen, das Grundprinzip der Therapie ohne Vorwissen zu verstehen – denn methodisch unterscheidet sich dieses Vorgehen deutlich von klassischen Dauermedikations‑Regimen. 1. Die Therapieform: Intervalltherapie + Bupropion (praxisnah erklärt)
1. Die Therapieform: Intervalltherapie + Bupropion (praxisnah erklärt)
1.1 Grundidee
Die Intervalltherapie basiert auf einem einfachen, aber wirkungsvollen Prinzip:
Stabilisierung durch gezielte Eingriffe – nicht durch Dauerblockade.
Aripiprazol wird nicht dauerhaft, sondern zeitlich begrenzt eingesetzt. In diesen Phasen dient es dazu, Denkprozesse zu ordnen, Schlaf zu stabilisieren und beginnende Frühwarnsymptome zuverlässig zu stoppen. Sobald diese Ziele erreicht sind, wird das Antipsychotikum wieder abgesetzt.
Bupropion hingegen wird kontinuierlich eingesetzt. Es übernimmt die tragende Rolle in den antipsychotikafreien Phasen, indem es Motivation, Kognition und Stressverarbeitung stabilisiert. Dadurch werden lange stabile Intervalle ohne Antipsychotikum überhaupt erst möglich.
Begleitend kommen – je nach Bedarf – SSRI, trizyklische Antidepressiva in Tropfenform, Trazodon sowie ausgewählte Nahrungsergänzungen zum Einsatz. Diese adressieren gezielt emotionale, vegetative und schlafbezogene Aspekte, die insbesondere in den Absetzphasen relevant werden.
Das übergeordnete Ziel ist eine funktionelle Stabilität ohne Dauerblockade – mit möglichst hoher Lebensqualität.
Zeitverlauf – Grundmedikation
1.2 Zeiträume der Intervalltherapie
Die Zeiträume der Intervalltherapie sind nicht starr, sondern funktionell begründet und individuell anpassbar.
Aripiprazol‑Phase
Diese Phase dauert typischerweise ca. 1,5–3 Wochen. Sie wird so lange fortgeführt, bis Schlaf, Denktempo und Frühwarnsymptome vollständig stabilisiert sind. Entscheidend ist nicht die Dauer, sondern das Erreichen dieses stabilen Zustands.
Absetzphase
Nach Absetzen des Antipsychotikums folgt eine Phase von ca. 2–8 Monaten, in der Bupropion die Stabilität trägt. In dieser Zeit ist keine antipsychotische Dauertherapie notwendig.
Dynamik über die Jahre
Zu Beginn der Therapie sind die Absetzintervalle häufig länger und liegen bei ca. 6–12 Monaten. Mit zunehmender Stabilisierung verkürzen sich diese Intervalle oft auf ca. 2–6 Monate.
Wichtig:
Diese Verkürzung ist kein Rückschritt, sondern ein Zeichen von:
- nachlassender Rezeptorsensitivität
- besserer dopaminerger Integration
- höherer funktioneller Belastbarkeit unter Bupropion
 ASCII‑Diagramm: IntervallzyklusCode:
ASCII‑Diagramm: IntervallzyklusCode:┌──────────────────────────────┐ │ Aripiprazol-Phase │ │ (ca. 1,5–3 Wochen) │ └──────────────┬──────────────┘ Reset ↓ ┌──────────────────────────────────────────┐ │ Absetzphase ohne Antipsychotikum │ │ (ca. 2–8 Monate) │ │ Beginn: 6–12 Monate │ │ später: 2–6 Monate │ └──────────────────────────────────────────┘ ↑ │ Frühwarnsymptome
1.3 Warum funktioniert das? (Kurzüberblick)
Das Zusammenspiel der eingesetzten Wirkstoffe folgt einer klaren funktionellen Logik:
Aripiprazol sorgt kurzfristig für Ordnung im dopaminergen System und stabilisiert den Schlaf.
Bupropion verbessert langfristig Motivation, Kognition und Stressverarbeitung.
SSRI glätten emotionale Übersteuerungen und vegetative Begleitsymptome.
Trizyklische Tropfen sichern den Schlaf in sensiblen Phasen.
Ergänzungen unterstützen vegetative und neuroinflammatorische Achsen.
Gemeinsam ermöglichen sie stabile Phasen ohne dauerhafte Antipsychotika‑Belastung.
1.4 Was passiert in der Aripiprazol‑Phase?
Während der Aripiprazol‑Phase normalisiert sich das Denktempo, der Schlaf stabilisiert sich, Reizbarkeit nimmt ab und Fehlinterpretationen gehen deutlich zurück. Viele Betroffene berichten, dass sich das innere Erleben „ordnet“.
Ein zentraler Effekt ist der funktionelle Reset:
Antidepressiva, die zuvor an Wirkung verloren hatten, entfalten erneut ihre stabilisierende Wirkung. Auch Bupropion erhält dadurch ein neues therapeutisches Wirkfenster.
1.5 Was passiert in der Absetzphase?
In der Absetzphase übernimmt Bupropion die tragende Rolle. Es stabilisiert Motivation, Kognition und Stressverarbeitung. SSRI dämpfen emotionale Übersteuerungen, während trizyklische Tropfen den Schlaf sichern.
Das Denktempo steigt in dieser Phase langsam an – ein Zeichen zunehmender funktioneller Aktivität. Nach mehreren Monaten sollte erneut ein Punkt erreicht werden, an dem ein weiterer kurzer Aripiprazol‑Einsatz funktionell angezeigt ist.
Dieses Kapitel gibt einen übersichtlichen, praxisnahen Überblick, ohne in mechanistische Details abzutauchen. 2. Die Wirkstoffe im Überblick (praxisnah)
2. Die Wirkstoffe im Überblick (praxisnah)
2.1 Aripiprazol (kurzzeitig)
Aripiprazol wirkt als Partialagonist und eignet sich besonders für kurze, gezielte Phasen. Es ordnet Denkprozesse, reduziert Überaktivierung, stabilisiert den Schlaf und dämpft Stressreaktivität. Seine Wirkung setzt rasch ein, was es ideal für die Intervalltherapie macht.
2.2 Bupropion (kontinuierlich)
Bupropion stabilisiert die präfrontale Dopaminversorgung, reduziert innere Unruhe und Reizbarkeit und verbessert Motivation sowie Kognition. Es trägt die antipsychotikafreien Phasen und ist damit zentrales Element der Therapie – nicht bloße Begleitmedikation.
2.3 SSRI
SSRI sind funktionell wichtig zur Dämpfung emotionaler Überladung, zur Regulation von Libido sowie zur Behandlung vegetativer Symptome wie Miktionsstörungen oder Verstopfung, die insbesondere in Absetzphasen auftreten können.
2.4 Trizyklische Tropfen (Trimipramin, Doxepin)
In sehr niedriger Tropfenform eingesetzt, sind sie ideal zur Schlafstabilisierung. Ihre Wirkung hält oft bis spät in die Absetzphase hinein an.
2.5 Trazodon
Trazodon wirkt mild sedierend und serotonerg stabilisierend und eignet sich besonders bei leichter Unruhe oder Einschlafstörungen.
2.6 Ergänzungen (kurz)
Vitamin B6 kann Unruhe und Akathisie lindern, Magnesium stabilisiert das GABA‑System, der B‑Komplex unterstützt vegetative Funktionen, Sulforaphan wirkt entzündungsmodulierend, und Lithium‑Orotat kann später Denküberlastung dämpfen.
Nachdem die Therapieform klar ist, lassen sich die zugrunde liegenden Mechanismen verständlich einordnen. 3. Mechanismen (einfach, getrennt, dann zusammengeführt)
3. Mechanismen (einfach, getrennt, dann zusammengeführt)
3.1 NET – Noradrenalin
Die Modulation des Noradrenalin‑Transporters reduziert Stressreaktivität, Reizbarkeit, Impulsivität und emotionale Überladung. Dies ist ein zentraler Beitrag zur inneren Stabilität in den Absetzphasen.
3.2 DAT – Dopamin
Die Dopamin‑Modulation verbessert Motivation, Kognition und Integration. Sie reduziert Fehlinterpretationen und wirkt damit sowohl auf Negativ‑ als auch auf Positivsymptome stabilisierend.
3.3 Partialagonismus (Aripiprazol)
Aripiprazol ordnet Denkprozesse, stabilisiert den Schlaf, reduziert Überaktivierung und verhindert eine vollständige Blockade dopaminerger Signalwege. Dadurch bleibt funktionelle Flexibilität erhalten.
3.4 Zusammenspiel
NET beruhigt,
DAT integriert,
Aripiprazol ordnet.
→ Stabilität ohne Dauerblockade
Nachdem die Therapieform und die beteiligten Wirkstoffe beschrieben wurden, stellt sich die zentrale Frage: 4. Intervalllogik – warum dieses Modell funktioniert
4. Intervalllogik – warum dieses Modell funktioniert
Warum ist gerade diese zeitliche Struktur wirksam – und warum ist sie klassischen Dauertherapien in bestimmten Fällen überlegen?
Die Antwort liegt nicht in einzelnen Wirkstoffen, sondern in der Dynamik zwischen Aktivierung, Ordnung und Adaptation des zentralen Nervensystems.
4.1 Warum kurze Aripiprazol‑Phasen ausreichen
Aripiprazol unterscheidet sich grundlegend von klassischen Antipsychotika. Als Partialagonist wirkt es nicht primär blockierend, sondern regulierend. Bereits nach kurzer Einnahme kommt es zu einer deutlichen Ordnung dopaminerger Signalverarbeitung.
Klinisch zeigt sich dies durch:
- rasche Normalisierung des Denktempos
- Rückgang von Fehlinterpretationen
- deutliche Schlafstabilisierung
- Reduktion innerer Spannung und Reizbarkeit
Deshalb reichen 1,5–3 Wochen in der Regel aus, um den gewünschten Reset zu erzielen.
4.2 Warum lange Absetzphasen möglich sind
Nach Absetzen des Antipsychotikums übernimmt Bupropion die tragende Rolle. Durch seine Wirkung auf Noradrenalin‑ und Dopamin‑Wiederaufnahme stabilisiert es genau jene Hirnregionen, die für Motivation, kognitive Integration und Stressverarbeitung entscheidend sind.
In dieser Phase:
- bleibt das Denktempo funktionell erhöht, aber kontrolliert
- verbessert sich die Alltagsfunktion
- nehmen Negativsymptome weiter ab
- bleibt die Positivsymptomatik meist auf Residualniveau
4.3 Warum sich die Intervalle im Verlauf verkürzen
Ein häufig missverstandener Punkt ist die Beobachtung, dass sich die Absetzintervalle im Verlauf der Therapie verkürzen können. Intuitiv wird dies oft als Verschlechterung interpretiert – funktionell ist jedoch meist das Gegenteil der Fall.
Mit zunehmender Stabilisierung:
- steigt das kognitive Funktionsniveau
- nimmt die dopaminerge Integration zu
- sinkt die Rezeptorsensitivität
- wird das System insgesamt belastbarer
Das Gehirn arbeitet auf einem höheren Aktivitätsniveau, wodurch der Punkt, an dem ein erneuter Reset sinnvoll wird, früher erreicht wird. Die Intervalle verkürzen sich typischerweise von anfänglich 6–12 Monaten auf 2–6 Monate.
Diese Verkürzung ist daher kein Rückschritt, sondern Ausdruck eines funktionellen Fortschritts.
4.4 Warum dies ein therapeutischer Fortschritt ist
Im Gegensatz zu klassischen Dauertherapien entsteht hier keine zunehmende Abhängigkeit von einer konstanten D2‑Blockade. Stattdessen bleibt das System adaptiv.
Langfristig bedeutet das:
- geringerer Bedarf an Antipsychotika
- bessere Erhaltung kognitiver Funktionen
- höhere Lebensqualität
- geringeres Risiko funktioneller Supersensitivität
4.5 Warum Antidepressiva „resetten“
Ein zentrales klinisches Phänomen ist, dass Antidepressiva – insbesondere Bupropion – nach einer Aripiprazol‑Phase wieder deutlich besser wirken.
Der Grund liegt nicht in pharmakokinetischen Effekten, sondern in der Verlangsamung des Denktempos und der Wiederherstellung eines stabilen adrenergen Gleichgewichts. Das therapeutische Wirkfenster verschiebt sich zurück in einen Bereich, in dem die antidepressiven Effekte wieder greifen können.
4.6 Warum Bupropion irgendwann „zu wenig“ wird
Mit zunehmender Aktivierung und Integration steigt das Denktempo weiter an. Irgendwann wird der Punkt erreicht, an dem selbst Bupropion die zunehmende Dynamik nicht mehr ausreichend modulieren kann.
Typische Zeichen sind:
- zunehmende Einschlafstörungen
- innere Unruhe trotz stabiler Tagesstruktur
- leichte Reizbarkeit
- beginnende Frühwarnsymptome
Dies ist kein Versagen von Bupropion, sondern ein Hinweis darauf, dass Aripiprazol kurzfristig für 1,5-3 Wochen stabilisierend und zum Antidepressiva-Resset benötigt wird.
Später kann auch Lithium-Orotate kontinuierlich eingenommendurch Sedierung zu einem funktioniellen Ersatz des Aripiprazols werden.
Einnahmeintervalle können sich damit verlängern und Denkbeschleunigungen normalisieren, sodass die Antidepressiva auch Bupropion länger wirksam sind.
4.7 Warum Schlafstörungen ein Frühwarnsignal sind
Schlafstörungen sind in diesem Modell kein isoliertes Symptom, sondern ein hoch sensitiver Marker für zunehmende Überaktivierung. Sie treten häufig vor einer deutlichen Verschlechterung der Positivsymptomatik auf.
Gerade deshalb sind sie ein zentrales Kriterium für den Zeitpunkt der erneuten Aripiprazol‑Einnahme.
4.8 Warum sich die Symptome nach dem Reset wieder beruhigen
Nach erneuter kurzer Aripiprazol‑Einnahme:
- verlangsamt sich das Denktempo
- stabilisiert sich der Schlaf
- normalisiert sich das adrenerge Gleichgewicht
- wird das Wirkfenster der Antidepressiva wiederhergestellt
Die Rolle von Nahrungsergänzungsmitteln ist in diesem Modell klar begrenzt. Sie ersetzen keine Medikation, können aber gezielt funktionelle Schwachstellen stabilisieren. 5. Nahrungsergänzung – funktionell und gezielt eingesetzt
5. Nahrungsergänzung – funktionell und gezielt eingesetzt
5.1 Vitamin B6
Vitamin B6 kann insbesondere bei Akathisie und innerer Unruhe hilfreich sein. Zusätzlich wird häufig eine deutliche Appetitreduktion beobachtet, was bei Schizophrenie relevant sein kann, da hier nicht selten ein übermäßiger Appetit besteht.
Wichtig ist jedoch die zeitliche Begrenzung höherer Dosierungen. Bei längerer Einnahme können periphere Neuropathien auftreten, die als klinischer Marker für eine Pause oder Dosisreduktion dienen.
5.2 Magnesium
Magnesium unterstützt die GABAerge Hemmung und wirkt stabilisierend auf das vegetative Nervensystem. Es kann insbesondere bei innerer Spannung und Schlafproblemen hilfreich sein.
5.3 B‑Komplex
Ein B‑Komplex unterstützt allgemeine vegetative Funktionen und kann insbesondere in Phasen erhöhter Belastung sinnvoll sein.
5.4 Sulforaphan
Sulforaphan wirkt entzündungsmodulierend und kann neuroinflammatorische Prozesse günstig beeinflussen. Seine Rolle ist unterstützend, nicht zentral.
5.5 Lithium‑Orotat
Lithium‑Orotat wird in diesem Modell nicht früh, sondern erst nach Jahren stabiler Intervalltherapie relevant. In sehr niedrigen Mikrodosierungen kann es Denküberlastung dämpfen und dadurch helfen, die Absetzphasen weiter zu verlängern.
Es kann damit langfristig eine funktionelle Ergänzung darstellen, ersetzt jedoch nicht die ordnende Wirkung von Aripiprazol in akuten Phasen.
Nachdem die praktische Anwendung, die Intervalllogik und die zentralen Wirkmechanismen beschrieben wurden, lässt sich das Modell nun in eine übergeordnete funktionelle Ordnung einbetten. Diese ist entscheidend, um zu verstehen, warum die Intervalltherapie nicht nur symptomatisch wirkt, sondern langfristig stabilisierend sein kann. 6. Funktionelle Gesamtordnung – die „große Landkarte“
6. Funktionelle Gesamtordnung – die „große Landkarte“
6.1 Dopamin – Salienz, Integration und Denktempo
Dopamin ist nicht primär ein „Psychose‑Neurotransmitter“, sondern ein Regulator von Bedeutung und Integration. Es steuert, welche Reize als relevant wahrgenommen werden und wie Informationen miteinander verknüpft werden.
In der Schizophrenie finden sich häufig zwei parallele Zustände:
- eine präfrontale Unterversorgung, die zu Antriebslosigkeit, kognitiven Defiziten und Negativsymptomen führt
- eine mesolimbische Überreaktivität, die Fehlinterpretationen und Positivsymptome begünstigt
Bupropion verstärkt dopaminerge Signalübertragung dort, wo sie funktionell fehlt, während Aripiprazol in akuten Phasen überschießende Aktivität ordnet, ohne das System dauerhaft zu blockieren.
6.2 Noradrenalin – Stress, Reizbarkeit und Impulsivität
Noradrenalin ist eng mit Stressverarbeitung, Wachheit und Impulskontrolle verbunden. Entscheidend ist dabei nicht die absolute Aktivität, sondern das Verhältnis der adrenergen Rezeptoren.
Ein funktionell stabiles System zeichnet sich durch folgende Reihenfolge aus:
α2 > α1 > β
- α2‑Dominanz wirkt beruhigend und regulierend
- α1‑Übergewicht führt zu innerer Unruhe, Reizbarkeit und Kontrollverlust
- β‑Aktivität verstärkt körperliche Stressreaktionen
Aripiprazol kann in akuten Phasen das Gleichgewicht rasch wiederherstellen, wenn es durch zunehmende psychotische Dynamik gekippt ist.
6.3 Glutamat – Präzision und Vorhersagefehler
Glutamat steuert die Präzision neuronaler Signalverarbeitung. In der Schizophrenie kommt es häufig zu einer fehlerhaften Gewichtung von Vorhersagefehlern: Unwichtige Reize erhalten zu viel Bedeutung, während relevante Informationen nicht ausreichend integriert werden.
Die indirekte Stabilisierung dopaminerger und noradrenerger Systeme wirkt hier regulierend. Eine verbesserte Integration reduziert die glutamaterge Übersteuerung, ohne direkt in dieses System einzugreifen.
6.4 GABA – Hemmung und Stabilität
GABA ist der wichtigste inhibitorische Neurotransmitter. Eine ausreichende GABAerge Hemmung ist Voraussetzung für innere Ruhe, Schlaf und emotionale Stabilität.
Magnesium und trizyklische Antidepressiva in sehr niedriger Dosierung unterstützen diese Achse funktionell. Sie wirken nicht antipsychotisch im engeren Sinne, tragen aber wesentlich zur Stabilität in sensiblen Phasen bei.
6.5 Neuroinflammation – ein modulierender Faktor
Zunehmend wird deutlich, dass neuroinflammatorische Prozesse den Verlauf psychotischer Erkrankungen beeinflussen können. Sie wirken nicht als primäre Ursache, können aber bestehende Dysbalancen verstärken.
Sulforaphan wird in diesem Modell als unterstützende Maßnahme eingeordnet, um entzündliche Prozesse zu modulieren. Seine Rolle ist ergänzend, nicht zentral.
6.6 Rezeptorsensitivität – Anpassung statt Fixierung
Ein zentrales Ziel der Intervalltherapie ist die Vermeidung funktioneller Supersensitivität. Dauerhafte D2‑Blockade kann zu einer Hochregulation von Rezeptoren führen, was langfristig die Rückfallneigung erhöht.
Durch die zeitlich begrenzte Anwendung von Aripiprazol bleibt das System adaptiv.
Diese Überlegung wird durch die Einschätzung von Stephen M. Stahl gestützt, der die Prävention dopaminerger Supersensitivität als plausiblen Nutzen dieser Strategie beschreibt.
Die im Anhang dargestellte Tabelle bietet eine vergleichende Übersicht über Nebenwirkungsprofile atypischer Antipsychotika. Sie dient nicht der direkten Therapieentscheidung, sondern der Einordnung, warum Aripiprazol für dieses Modell besonders geeignet ist. 7. Nebenwirkungsprofile atypischer Antipsychotika
7. Nebenwirkungsprofile atypischer Antipsychotika
Im Vergleich zeigt sich:
- geringere metabolische Belastung
- geringere Sedierung
- geringere Prolaktinwirkung
- gute kognitive Verträglichkeit
Die hier beschriebene Intervalltherapie stellt kein alternatives Heilversprechen dar, sondern eine funktionelle Weiterentwicklung etablierter Behandlungsansätze. 8. Fazit – ein funktionelles Weiterdenken klassischer Therapie
8. Fazit – ein funktionelles Weiterdenken klassischer Therapie
Sie ermöglicht:
- Stabilität ohne dauerhafte Antipsychotika‑Belastung
- bessere Versorgung von Negativ‑ und kognitiven Symptomen
- höhere Lebensqualität
- langfristig günstigere Verläufe
- eine plausible Prävention funktioneller Supersensitivität
Kontinuierliche Einnahme von Bupropion (NDRI)
Bupropion gehört zur Klasse der Noradrenalin‑Dopamin‑Wiederaufnahmehemmer (NDRI) und unterscheidet sich in seinem Wirkprofil deutlich von trizyklischen Antidepressiva. Während trizyklische Substanzen unspezifisch mehrere Rezeptorsysteme beeinflussen, wirkt Bupropion vergleichsweise selektiv auf Noradrenalin‑ und Dopamin‑Transporter.
Durch die kontinuierliche Wiederaufnahmehemmung entsteht ein funktionelles dopaminerges und noradrenerges „Grundrauschen“. Dieses reduziert extreme Schwankungen zwischen Mangel‑ und Überaktivierungszuständen und trägt zur Stabilisierung der Rezeptorsensitivität bei. Funktionell wirkt Bupropion damit nicht sedierend oder blockierend, sondern modulierend.
Wirkung auf Symptome
Klinisch zeigt sich die Wirkung von Bupropion insbesondere in folgenden Bereichen:
- Verbesserung von Kognition und Negativsymptomen
- Reduktion innerer Unruhe, Reizbarkeit und Impulsivität
- Stabilisierung der Stressverarbeitung
- Unterstützung beim Rauchstopp durch dopaminerge Wirkung
Antipsychotische Komponente im therapeutischen Fenster
Die antipsychotische Wirkung von Bupropion ist nicht akut und nicht blockierend. Sie entfaltet sich innerhalb eines therapeutischen Fensters, das durch kurzzeitige Aripiprazol‑Einnahmen regelmäßig neu hergestellt wird. In diesem Fenster wirkt Bupropion stabilisierend auf dopaminerge Netzwerke, insbesondere in präfrontalen Regionen, in denen häufig ein funktioneller Dopaminmangel besteht.
Gleichzeitig führt die kontinuierliche Wiederaufnahmehemmung zu einer funktionellen „Abstumpfung“ übersensibler Dopaminrezeptoren. Dies kann erklären, warum sich sowohl Negativ‑ als auch Positivsymptome im Verlauf der Absetzphasen häufig deutlich bessern.
NET‑Wirkung und innere Unruhe
Ein zentraler, oft missverstandener Aspekt ist die Wirkung von Bupropion auf innere Unruhe und Reizbarkeit. Diese Effekte sind primär auf die Noradrenalin‑Wiederaufnahmehemmung zurückzuführen.
Bupropion stabilisiert das adrenerge Gleichgewicht in Richtung eines funktionell günstigen Verhältnisses:
α2 > α1 > β
Dieses Verhältnis wirkt stressdämpfend, reduziert Impulsivität und innere Unruhe und verbessert die emotionale Kontrolle – ohne sedierend zu wirken. Berichte über „Unruhe als Nebenwirkung“ von Bupropion sind in diesem Kontext häufig irreführend. In der Intervalltherapie ist Unruhe meist ein Hinweis auf:
- eine zu niedrige Dosis
- eine ungünstige Tagesverteilung
- oder das Erreichen des nächsten Intervall‑Reset‑Punktes
Einnahmestruktur und Dosisentwicklung
Im Gegensatz zu depressiven Störungen muss Bupropion bei Schizophrenie sehr langsam eingeschlichen werden. Eine Steigerung innerhalb weniger Tage oder Wochen ist in diesem Kontext unpassend und führt häufig zu ausgeprägten Schlafstörungen.
Die Dosisentwicklung orientiert sich daher nicht an festen Zeitplänen, sondern an:
- Schlafqualität
- Verträglichkeit
- Stabilität der Absetzintervalle
- erstes Absetzintervall: niedrige Dosis
- zweites Absetzintervall: moderate Dosis
- weitere Intervalle: schrittweise Anpassung bei guter Verträglichkeit
Ab Dosierungen oberhalb von etwa 450 mg steigt das Risiko für Krampfanfälle, weshalb die langsame Anpassung essenziell ist.
Schlafstörungen und Abgrenzung zu Frühwarnsymptomen
Leichte Schlaf‑ und Einschlafstörungen sind insbesondere im ersten Jahr der Therapie häufig und Teil der funktionellen Anpassung. Sie lassen sich in dieser Phase gut mit niedrig dosierten trizyklischen Antidepressiva oder Trazodon abfangen.
Treten jedoch nach mehreren Monaten ohne Antipsychotikum erneut ausgeprägte Schlafstörungen auf, die sich trotz schlaffördernder Begleitmedikation nicht mehr kontrollieren lassen, handelt es sich häufig um ein Frühwarnsignal. In diesem Fall verlieren auch sedierende Antidepressiva und SSRI zunehmend ihre Wirkung – ein klares Zeichen für die Notwendigkeit einer erneuten kurzen Aripiprazol‑Phase.
 Medikamentenplan – funktionelle Übersicht
Medikamentenplan – funktionelle Übersicht1. Hauptmedikation – tragende Säulen der Intervalltherapie
Wirkstoff Substanzklasse Einsatz im Therapieverlauf Zentrale Funktion Aripiprazol Atypisches Antipsychotikum (Partialagonist) Kurzzeitig bei Frühwarnsymptomen, intervallweise Ordnung von Denkprozessen,
Schlafstabilisierung, Re‑Stabilisierung bei Positivsymptomen, Reset des therapeutischen FenstersBupropion NDRI‑Antidepressivum Kontinuierlich über Absetzphasen hinweg Funktionelle Ordnung durch verbesserte Kognition und Wahrnehmungsintegration, Stabilisierung von Kognition und Negativsymptomen, Reduktion innerer Unruhe und Reizbarkeit, indirekte antipsychotische Wirkung im Intervallmodell, Rauchstopp
2. Begleitmedikation – symptomorientierte Ergänzung
Wirkstoff Substanzklasse Typischer Einsatzbereich Funktioneller Nutzen Citalopram / Escitalopram SSRI‑Antidepressivum Absetzphasen ohne Antipsychotikum Dämpfung emotionaler Übersteuerung und Libido, Unterstützung bei Miktionsstörungen und Verstopfung, vegetative Stabilisierung Trimipramin Trizyklisches Antidepressivum (stark sedierend) Schlafstörungen, erhöhte Aktivierung Schlafinduktion, Sedierung, Schutz bei Suchtdynamiken Doxepin Trizyklisches Antidepressivum (mittel–stark sedierend) Schlafstörungen mit Tagesüberhang bei Trimipramin Schlafstabilisierung mit geringerer Residualsedierung Trazodon SARI‑Antidepressivum Leichte Schlafstörungen, milde Unruhe Sanfte Sedierung, serotonerge Stabilisierung, ggf. SSRI‑ähnlicher Ersatz
3. Nahrungsergänzung – funktionell priorisiert
Substanz Kategorie Einsatzschwerpunkt Funktioneller Nutzen Vitamin B6 Mikronährstoff Begleitend Reduktion innerer Unruhe und Akathisie, Appetitregulation Lithium‑Orotat Spurenelement (Mikrodosis kontinuierlich eigngenommen) Langfristig, nach Jahren stabiler Intervalltherapie, langfristiger Ersatz von Aripiprazol möglich Dämpfung von Denkbeschleunigung, Verlängerung der Absetzphasen Magnesium Mineralstoff Begleitend Unterstützung der GABA‑Achse, vegetative Stabilität B‑Komplex Vitaminkombination Begleitend Unterstützung vegetativer und metabolischer Prozesse Sulforaphan Pflanzenextrakt Begleitend Modulation neuroinflammatorischer Prozesse Vitamin D3 / Multivitamin Basisversorgung Ergänzend Allgemeine Unterstützung, keine zentrale therapeutische Rolle
 Sicherheitshinweis zu Vitamin B6: Höhere Dosierungen sollten nur zeitlich begrenzt erfolgen. Bei längerer Einnahme besteht ein Risiko für periphere Neuropathien, die als klinischer Marker für eine Pause oder Dosisreduktion dienen.
Sicherheitshinweis zu Vitamin B6: Höhere Dosierungen sollten nur zeitlich begrenzt erfolgen. Bei längerer Einnahme besteht ein Risiko für periphere Neuropathien, die als klinischer Marker für eine Pause oder Dosisreduktion dienen.
Autor & Verantwortung
Text und Redaktion: Markus („Maggi“) – Schizophrenie‑Forum.com
Schwerpunkte: Psychose‑Erfahrungen, funktionelle Therapieansätze, verständliche Darstellung wissenschaftlicher Inhalte.
Dieser Artikel wurde sorgfältig recherchiert und dient der Orientierung – er ersetzt keine medizinische Beratung.
 Artikel Druckansicht
Artikel Druckansicht -
Laden…
-
Laden…
